発作性夜間ヘモグロビン尿症(PNH)は、PIGAを含むGPIアンカー合成に関わる遺伝子に変異を有する造血幹細胞がクローン性に拡大して生じる、補体介在性血管内溶血を主徴とする造血幹細胞疾患です1)。
発作性夜間ヘモグロビン尿症(PNH)とは
発作性夜間ヘモグロビン尿症(PNH)の疫学
PNHの有症率は1999年の国内データでは100万人に3.6人となっており、2021年の海外データでは100万人に38.1人とされています。
性差については、近年の報告では地域によらず男女比がほぼ1:1 であるとされています1)。
主な先行病変は再生不良性貧血、骨髄異形成症候群があります。


表1:PNHの疫学
発作性夜間ヘモグロビン尿症(PNH)の生命予後
PNHは生命にかかわる進行性の難治性疾患です。
PNHの長期予後は、補体C5阻害剤の導入前後によって、大きく変化しています1)。
補体C5阻害剤の導入前
日米比較調査報告によると、診断後の平均生存期間は、日本が32.1年、アメリカは19.4年と差がある一方、50%生存期間では、それぞれ25.0 年、23.3 年と、統計的な有意差は得られていません(Kaplan-Meier法、p=0.7)(図1)1) 5)。


- 試験概要
- 日本と米国におけるPNHの臨床経過を比較することを目的に、PNHと診断され現病歴が明らかな患者(米国Duke Universityの176例、日本の26施設から登録された209例)を対象にデータを収集した。PNH診断後の生存期間は米国173例、日本177例を対象に解析し、生存率はKaplan-Meier法を用いて推定した。日米ともに患者の一部は副腎皮質ステロイド薬や輸血などによる治療を受けていた。
図1:日本とアメリカにおける診断後の生存率曲線(Kaplan-Meier 法)
補体C5阻害剤の導入後
フランスで行われたコホート研究によると、PNH患者の診断時点から6年時の生存率は、補体C5阻害剤治療群で92%、1985年以降に診断された患者群で80%、1950年~1984年に診断された患者群で58%でした(図2)8)。


- 試験概要
- フランスで2005年12月~2014年12月に補体C5阻害薬治療を受けたPNH患者123例と過去の自然史研究の対象であったフランスのレジストリに登録されたPNH患者(ヒストリカルコントロール)191例について、後方視的に比較した。ヒストリカルコントロールは、既報における生存率の差に基づき、1950~1984年に診断された患者(91例)と1985年以降に診断された患者(100例)に分けて解析した。全生存期間はKaplan-Meier法を用いて推定し、群間比較にはCox比例ハザードモデルを用いた。
- 【安全性】
- 死亡は補体C5阻害薬治療群で9例(Budd-Chiari症候群、造血幹細胞移植関連の合併症が各2例、出血、骨髄異形成症候群が各1例、不明が3例)に認められた。
図2:補体C5阻害剤治療を受けたPNH患者の生存率
(補体C5阻害剤登場以前の患者さんとの比較)(海外データ)
合併症、死亡のリスク因子
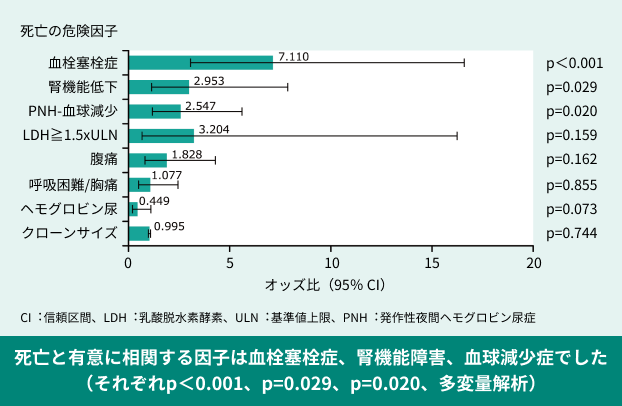
韓国PNHレジストリに登録されたPNH患者301例(補体C5阻害剤による治療を受けている患者は除外)の患者背景、病歴およびPNHに関する情報(赤血球と顆粒球クローンサイズ、症状と合併症、臨床検査値、治療、死亡の原因など)を後ろ向きに調査し、死亡の危険因子を単変量解析および多変量解析を用いて解析したところ、死亡と有意に相関する因子は血栓塞栓症、腎機能障害、血球減少症でした(図3)9)。

- 試験概要
- 韓国PNHレジストリに登録されたPNH患者301例(補体C5阻害剤治療を受けている患者は除外)の患者背景、病歴およびPNHに関する情報(⾚⾎球と顆粒球クローンサイズ、症状と合併症、臨床検査値、治療、死亡の原因など)を後ろ向きに調査し、死亡の危険因⼦を単変量解析および多変量解析を⽤いて解析した。
図3:死亡の危険因子についての単変量および多変量解析(海外データ)
また、フランスの予後因子の多変量解析(220 例)によると、以下の6項目が予後不良因子として示されています1)。(海外データ)
- 血栓症の発症:相対死亡危険率(RR=10.2)
- 汎血球減少症への進展(RR=5.5)
- 骨髄異形成症候群(MDS)/急性白血病の発症(RR=19.1)
- 診断時年齢55才以上(RR=4.0)
- 複数の治療必要症例(RR=2.1)
- 診断時の血小板減少(RR=2.2)
- RR:relative risk
補体カスケードと補体の役割
補体は自然免疫を構成する重要な要素であり、生体防御において多くの役割を果たします10)11)。
主要な補体因子は9つあり、C1~C9と表され、カスケード反応を起こし活性化します。
補体の活性化経路には「古典経路」「レクチン経路」「第二経路」の3つがあります(図4)。
いずれの経路も、C3転換酵素によってC3aとC3bに分解し、さらにはC5転換酵素によってC5が開裂し、C5aとC5bが生成されます。そしてC5bはC6~C9とともにMACを形成します。
近位補体であるC3bはオプソニン化や免疫複合体除去に関与します。侵入してきた病原体などに結合して標識すること(オプソニン化)により食細胞が病原体などを認識し、貪食、排除します。また病原体などの排除とともに免疫複合体の除去も行います。
C3は補体系の中で重要な因子のひとつであり、C3が欠損すると病原体感染に易感染性になるなど、さまざまな影響があらわれると考えられます。
終末補体であるC5aはC3aと同じく白血球を動員して活性化する作用を有し、その作用はC3aよりはるかに強いといわれています。
また、C5bとC6~C9からなるMACは、病原体の細胞膜を破壊し、細胞を融解します。


図4:PNHにおける補体カスケード
発作性夜間ヘモグロビン尿症(PNH)の主な病態
PNHでは、慢性的な補体介在性の血管内溶血が生じており1)、PNHの主病態は血管内溶血です。
終末補体から形成されたMAC(membrane attack complex、膜侵襲複合体)による赤血球の破壊が血管内溶血を引き起こします12)13)(図5)。
血管内溶血は貧血や疲労感などの症状だけでなく血栓症、腎障害、肺高血圧症といった生命予後に関わる合併症の要因になります12)13)。


図5:血管内溶血のイメージ
血管内溶血のメカニズム
図6に血管内溶血のメカニズム(イメージ)を示します。
PNHではGPIアンカー型タンパク欠損により慢性的な血管内溶血が起こっており14)-16)、常に活性化状態の補体系が、GPIアンカー型タンパクが欠損している異常な赤血球を攻撃しています15)16)。


図6:血管内溶血のメカニズムのイメージ
血管内溶血が引き起こす補体制御異常の影響
血管内溶血が生じた結果、PNH患者さんではヘモグロビン尿や貧血、呼吸困難などの症状が発現します。
また、血管内溶血によって血漿中に放出された遊離ヘモグロビンがNOと結合することで、血栓症や腎障害、肺高血圧症といった生命予後に関わる合併症を引き起こすこともあります(図7)17)-22)。
このように、血管内溶血はPNHの病態において中心的役割を果たし、さまざまな症状や生命を脅かす合併症の引き金となることから、PNHで最も重視すべき事象です20)21)。
血管内溶血を抑制することは、PNH患者さんの症状やQOLを改善するうえで、きわめて重要と考えられます。


図7:補体制御異常の影響
補体C5阻害剤治療中の患者さんの一部で顕性化する血管外溶血
PNHは、補体活性化反応の制御異常によって赤血球がMACにより破壊され、血管内溶血があらわれる疾患です23)。
補体C5阻害剤を用いたPNH治療は、MAC形成にかかわる補体C5を阻害し、血管内溶血を抑制することを目的としています。
しかし、補体C5阻害剤で治療中の一部のPNH患者さんで、血管内溶血を抑えているにもかかわらず、貧血症状が継続して輸血が必要となる場合があります。
その原因のひとつと考えられているのが血管外溶血です。
血管外溶血の影響
血管外溶血は血管内溶血とは異なる原因で発症します。したがって身体への影響も異なります。
補体C5阻害剤により血管内溶血が抑制された結果、一部の赤血球上にC3フラグメントが蓄積します。
C3フラグメントの働きにより、赤血球は食細胞からの貪食を受けやすくなり(オプソニン化)、脾臓や肝臓などで貪食されて血管外溶血を起こします24)(図8)。
血管外溶血によって、補体C5阻害剤で治療中のPNH患者さんに貧血や、貧血による疲労感・倦怠感、黄疸、胆石などの症状が残る可能性があります25)。
この血管外溶血は、過去15年以上にわたって支持的に管理され、生存率は健常人とほぼ変わらない状況まで改善しています26)。
劇的な臨床経過をたどることもある血管内溶血に比べ、血管外溶血は生命にかかわらないことが多い27)28)一方、患者さんのQOLに影響します。


図8:血管外溶血のイメージ
図8:血管外溶血のイメージ
血管外溶血の鑑別
PNHの主病態である血管内溶血の制御が達成された後も、症候性貧血が残存すれば、その原因を特定し、必要に応じて治療する必要があります。
補体C5阻害剤による治療後、残存するPNH赤血球の膜上にはC3フラグメントが蓄積することで、一部の患者さんで血管外溶血が顕性化します1)(図9)。
補体C5阻害剤による治療中の患者さんにおいて、治療が必要な血管外溶血の有無を判断する際には、貧血症状の有無、網状赤血球数、間接ビリルビン値などを参考にします。


図9:血管外溶血の調査鑑別
- 1)
- 発作性夜間ヘモグロビン尿症診療の参照ガイド 令和4 年度改訂版, 2023年3月.
- 2)
- 大野良之:「特定疾患治療研究事業未対象疾患の疫学像を把握するための調査研究班」平成11年度研究業績集-最終報告書-平成12年3月発行(2000年)
- 3)
- 難病情報センター(特定医療費(指定難病)受給者証所持者数(https://www.nanbyou.or.jp/)(2023年12月アクセス)より引用
- 4)
- Richards SJ, et al. Eur J Haematol. 2021;107(2):211-218.
- 5)
- Nishimura JI, et al. Medicine (Baltimore). 2004;83(3):193-207.
- 6)
- Borowitz MJ, et al. Cytometry B Clin Cytom. 2010;78(4):211-230.
[利益相反:本ガイドラインはAlexion Pharmaceuticals, Inc. の支援によって策定された。著者にAlexion Pharmaceuticals, Inc.の顧問が含まれる。著者にAlexion Pharmaceuticals, Inc.より研究助成金等を受領している者が含まれる。 ] - 7)
- Lee JW, et al. Int J Hematol. 2013;97(6):749-757.
[利益相反:本論文の著者にAlexion Pharmaceuticals, Inc.より講演料、顧問料等を受領している者が含まれる。 ] - 8)
- Loschi M, et al. Am J Hematol. 2016;91(4):366-370.
[利益相反:本論文の著者にAlexion Pharmaceuticals, Inc.の顧問が含まれる。 ] - 9)
- Jang JH, et al. J Korean Med Sci. 2016;31(2):214-221.
- 10)
- Walport MJ. N Engl J Med. 2001;344(14):1058-1066.
- 11)
- Murphy K. Janeway’s Immunobiology. 9th ed. New York, NY:Garland Science, Taylor & Francis Group, LLC;2016.
- 12)
- Notaro R, et al. N Engl J Med. 2022;387(2):160-166.
- 13)
- Kulasekararaj AG, et al. Ther Adv Hematol. 2022;13:20406207221091046.
[利益相反:本試験はAlexion, AstraZeneca Rare Disease, Inc. の支援によって実施された。著者の一部はAlexion, AstraZeneca Rare Disease, Inc. のadvisory board のメンバーである。また著者にAlexion, AstraZeneca Rare Disease, Inc. より顧問料、謝礼金、講演料、旅費、研究助成金を受領している者が含まれる。] - 14)
- Borowitz MJ, et al. Cytometry B Clin Cytom. 2010;78(4):211-230.
[利益相反:ガイドラインはAlexion, AstraZeneca Rare Disease, Inc. の支援によって策定された。著者にAlexion Pharmaceuticals, Inc.の顧問が含まれる。著者にAlexion Pharmaceuticals, Inc.より研究助成金等を受領している者が含まれる。] - 15)
- Parker CJ. Hematology Am Soc Hematol Educ Program. 2011:2011:21-29.
- 16)
- Parker CJ. Hematology Am Soc Hematol Educ Program. 2016;2016(1):208-216.
- 17)
- Kelly R, et al. Ther Clin Risk Manag. 2009;5:911-921.
[利益相反:本論文の著者にAlexion Pharmaceuticals, Inc. より研究助成金、講演料、顧問料を受領している者が含まれる。] - 18)
- Rother RP, et al. JAMA. 2005;293(13):1653-1662.
[利益相反:本論文の著者にAlexion Pharmaceuticals, Inc. の社員及び顧問が含まれる。著者にAlexion Pharmaceuticals, Inc. より研究助成金を受領している者が含まれる。] - 19)
- Hill A, et al. Blood. 2013;121(25):4985-4996.
[利益相反: 本論文の著者はAlexion Pharmaceuticals, Inc. より謝礼金、研究助成金を受領している。] - 20)
- Zatz R, et al. Hypertension. 1998;32(6):958-964.
- 21)
- Rachidi S, et al. Eur J Intern Med. 2010;21(4):260-267.
- 22)
- Hill A, et al. Br J Haematol . 2010;149(3):414-425.
[利益相反:本試験はAlexion Pharmaceuticals, Inc. の支援によって実施された。 - 23)
- Luzzatto L, et al. Haematologica. 2010;95(4):523-526.
[利益相反:本論文の著者にAlexion Pharmaceuticals, Inc. より講演料、研究助成金、顧問料を受領している者が含まれる。 - 24)
- Risitano AM, et al. Blood. 2009;113(17):4094-4100.
[利益相反:本試験はAlexion Pharmaceuticals, Inc. によって実施された。著者にAlexion Pharmaceuticals, Inc. より講演料、研究助成金を受領している者が含まれる。
【監修】大阪大学大学院 医学系研究科 血液・腫瘍内科学
招聘教授 西村 純一 先生
作成年月:2024年9月
- 関係する外部機関へのリンクはコチラ


