高リスク患者群
PNH患者さんの適切な治療と長期予後のためには早期診断が重要です2,5
IDA:鉄欠乏性貧血、MDS:骨髄異形成症候群
*
まれな部位とは、肝静脈(バッド・キアリ症候群)、他の腹腔内静脈(門脈、脾静脈、内臓静脈)、脳静脈洞、皮膚静脈など。
- 国際臨床サイトメトリー学会(ICCS)ガイドラインおよび他の複数の専門家により、PNHのリスクの高い患者集団が明らかにされています1-4,6-20
- PNH型血球を同定することは、予後や治療の判定に重要です8,21
- ICCSガイドラインとIPIGは、PNHリスクの高い患者さんの継続的なモニタリングを推奨しています2.8
- 『発作性夜間ヘモグロビン尿症診療の参照ガイド 令和4年度改訂版』では「PNHタイプ赤血球(Ⅱ型+Ⅲ型)が1%以上」かつ「血清LDH値が正常上限の1.5倍以上」を満たす場合、PNHと診断するとされています9
※高感度フローサイトメトリーは保険適用外です。
ICCS:International Clinical Cytometry Society
IPIG:International PNH Interest Group
1. Rachidi S, et al. Eur J Intern Med. 2010;21(4):260-267. 2. Borowitz MJ, et al. Cytometry B Clin Cytom. 2010;78(4):211-230.[利益相反:本ガイドラインはAlexion Pharmaceuticals, Inc.の支援によって策定された。著者にAlexion Pharmaceuticals, Inc.の顧問が含まれる。著者にAlexion Pharmaceuticals, Inc.より研究助成金等を受領している者が含まれる。] 3. Hillmen P, et al. Am J Hematol. 2010;85(8):553-559.[利益相反:本論文の著者にAlexion Pharmaceuticals, Inc.の社員が含まれる。著者にAlexion Pharmaceuticals, Inc.の顧問、諮問委員会のメンバーが含まれる。著者に研究助成金を受領している者が含まれる。] 4. Brodsky RA. Paroxysmal nocturnal hemoglobinuria. In: Hoffman R, Benz EJ, Jr., Shattil SJ, et al. eds. Hematology: Basic Principles and Practice. 4th ed. Philadelphia: Elsevier; 2005:419-427. 5. Richards SJ, et al. Clin Lab Med. 2007;27(3):577-590. 6, Rother RP, et al. JAMA. 2005;293(13):1653-1662.[利益相反:本論文の著者にAlexion Pharmaceuticals, Inc.の社員及び顧問が含まれる。著者にAlexion Pharmaceuticals, Inc.より研究助成金を受領している者が含まれる。] 7. Hill A, et al. Blood. 2013;121(25):4985-4996.[利益相反:本論文の全著者はAlexion Pharmaceuticals, Inc.の諮問委員会のメンバーであり、Alexion Pharmaceuticals, Inc.より謝礼金等を受領している。] 8. Parker C, et al. Blood. 2005;106(12):3699-3709. 9. 発作性夜間ヘモグロビン尿症診療の参照ガイド 令和4年度改訂版, p4. 10. Raza A, et al. Cytometry B Clin Cytom. 2014;86(3):175-182. 11. Meyers G, et al. Int J Hematol. 2003;77(2):125-132. 12. Mohanty BD, et al. Am J Med. 2012;125(3):243-245.[利益相反:本論文の著者にAlexion Pharmaceuticals, Inc.の顧問が含まれる。] 13. Sharma VR. Clin Adv Hematol Oncol. 2013;11 Suppl 13(9):2-8.[利益相反:本論文はAlexion Pharmaceuticals, Inc.より提供された知見に基づいて作成された。著者にAlexion Pharmaceuticals, Inc.の社員が含まれる。] 14. de Latour RP, et al. Blood. 2008;112(8):3099-30106. 15. Brodsky RA. Blood. 2009;113(26):6522-6527.[利益相反:本論文の著者にAlexion Pharmaceuticals, Inc.の諮問委員会のメンバーが含まれる。] 16. National Comprehensive Cancer Network. NCCN Clinical Practice Guidelines in Oncology: Myelodysplastic syndromes. Version 1.2023. http://www.nccn.org/professionals/physician_gls/pdf/mds.pdf(2023年5月アクセス) 17. Ballarín J, et al. Nephrol Dial Transplant. 2011;26(10):3408-11. 18. Dolezel Z, et al. Pediatr Nephrol. 2004;19(10):1177-1179. 19. Parker CJ. Hematology Am Soc Hematol Educ Program. 2008:93-103. 20. Brodsky A, et al. Exp Hematol Oncol. 2012;1(1):26.[利益相反:本論文の著者にAlexion Pharmaceuticals, Inc.の社員及び顧問が含まれる。] 21. Dunn DE, et al. Ann Intern Med. 1999;131(6):401-408.
PNH患者さんにおける腎機能障害の有病率は、一般集団と比較して6.6倍高くなりました2,8(海外データ)
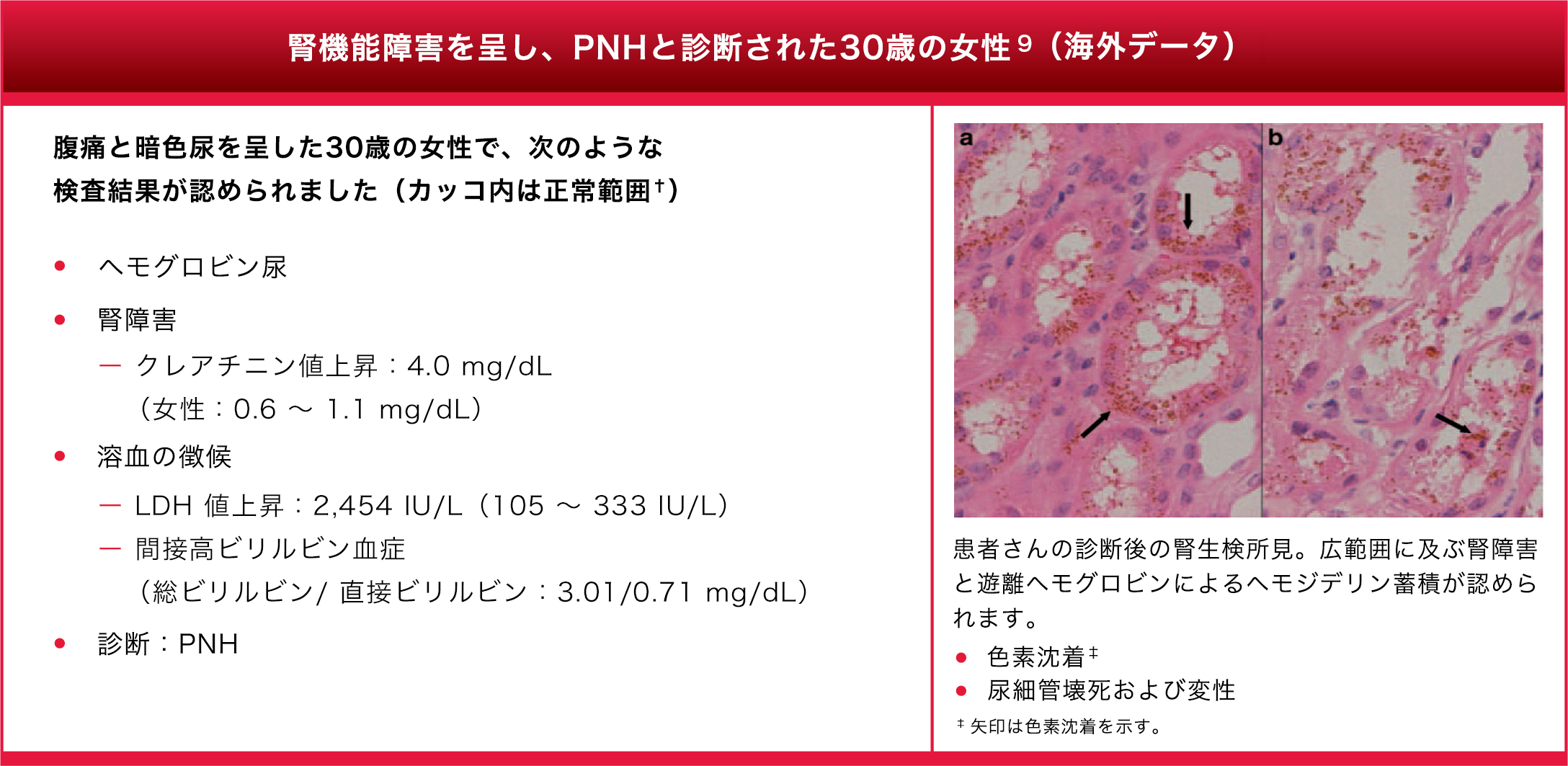
* 既報の症例研究から引用した 9。
† 正常範囲は MedlinePlusに基づく。検査施設間で若干異なる可能性がある。
PNHの早期診断が患者さんの長期予後に影響を与えます1,3
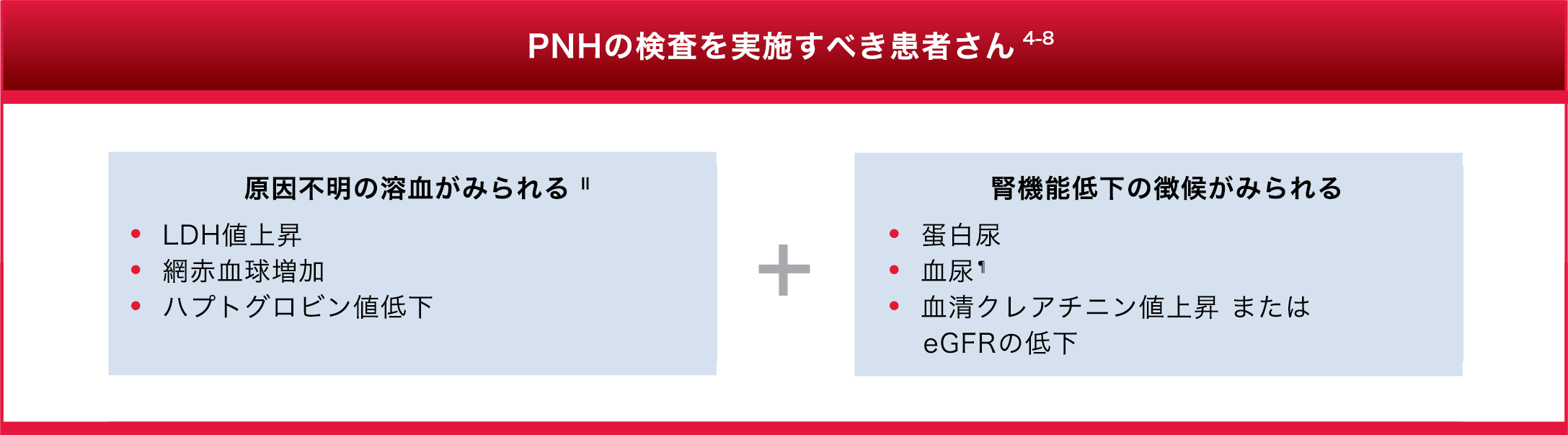
§ ここに示す情報は医療従事者の学習を目的とする。医療従事者による判断または臨床診断に代わるものではない。
Ⅱ 溶血の明らかな原因とは、手術中における血液への物理的な処置、感染症、ある種の薬剤投与、鎌状赤血球症などである4,11。
¶ ヘモグロビン尿と血尿の鑑別を怠ると、PNHの診断が遅れる大きな原因となる。詳細な泌尿器系検査が行われた後に、初めてヘモグロビン尿と血尿が鑑別される場合も多い10。
上記の判定基準を踏まえてPNHの疑いがあれば、高感度フローサイトメトリーを行ってください1
※高感度フローサイトメトリーは保険適用外です。
1. Borowitz MJ, et al. Cytometry B Clin Cytom. 2010;78:211-230 2. Hillmen P, et al. Am J Hematol. 2010;85:553-559. 3. Richards SJ, et al. Clin Lab Med. 2007;27:577-590. 4. Rother RP, et al. JAMA. 2005;293:1653-1662. 5. Baumgarten M, et al. Am Fam Physician. 2011;84:1138-1148. 6. Kato GJ, et al. Blood. 2006;107:2279-2285. 7. 発作性夜間ヘモグロビン尿症診療の参照ガイド 令和4年度改訂版, p22-23. 8. Stevens LA, et al. N Engl J Med. 2006;354:2473-2483. 9. Tsai CW, et al. Kidney Int. 2007;71:1187. 10. Parker CJ. Am Soc Hematol Educ Program. 2008:93-103. 11. Rosse WF. Paroxysmal nocturnal hemoglobinuria. In: Hoffman R, Benz EJ Jr, Shattil SJ, et al. eds. Hematology: Basic Principles and Practice. 3rd ed. New York, NY: Churchill Livingstone; 2000:331-342.
再生不良性貧血(AA)の患者さんはPNHのリスクが高くなります1-3
.png)
AA患者さんにおいてPNH型血球数は、時間の経過とともに急速かつ予測不能に増加することがあります1,3,5-6。
- AA患者さんの骨髄環境が、PNH型血球の拡大を促進することがあります2,7-8
1. Borowitz MJ, et al. Cytometry B Clin Cytom. 2010;78:211-230 2. Brodsky RA. Paroxysmal nocturnal hemoglobinuria. In: Hoffman R, Benz EJ, Jr., Shattil SJ, et al. eds. Hematology: Basic Principles and Practice. 4th ed. Philadelphia: Elsevier; 2005:419-427. 3. Parker C, et al. Blood. 2005;106:3699-3709. 4. Sugimori C, et al. Br J Haematol. 2009;147:102-112. 5. Raghupathy R, et al. Case Rep Hematol. 2012;2012:106182. 6. Pu JJ, et al. Eur J Haematol. 2011;87:37-45. 7. Kinoshita T, et al. Int J Hematol. 2002;75:117-122. 8. Tiu R, et al. Leukemia. 2007;21:1648-1657.
原因不明の血球減少の患者さんはPNHのリスクが高くなります1-2
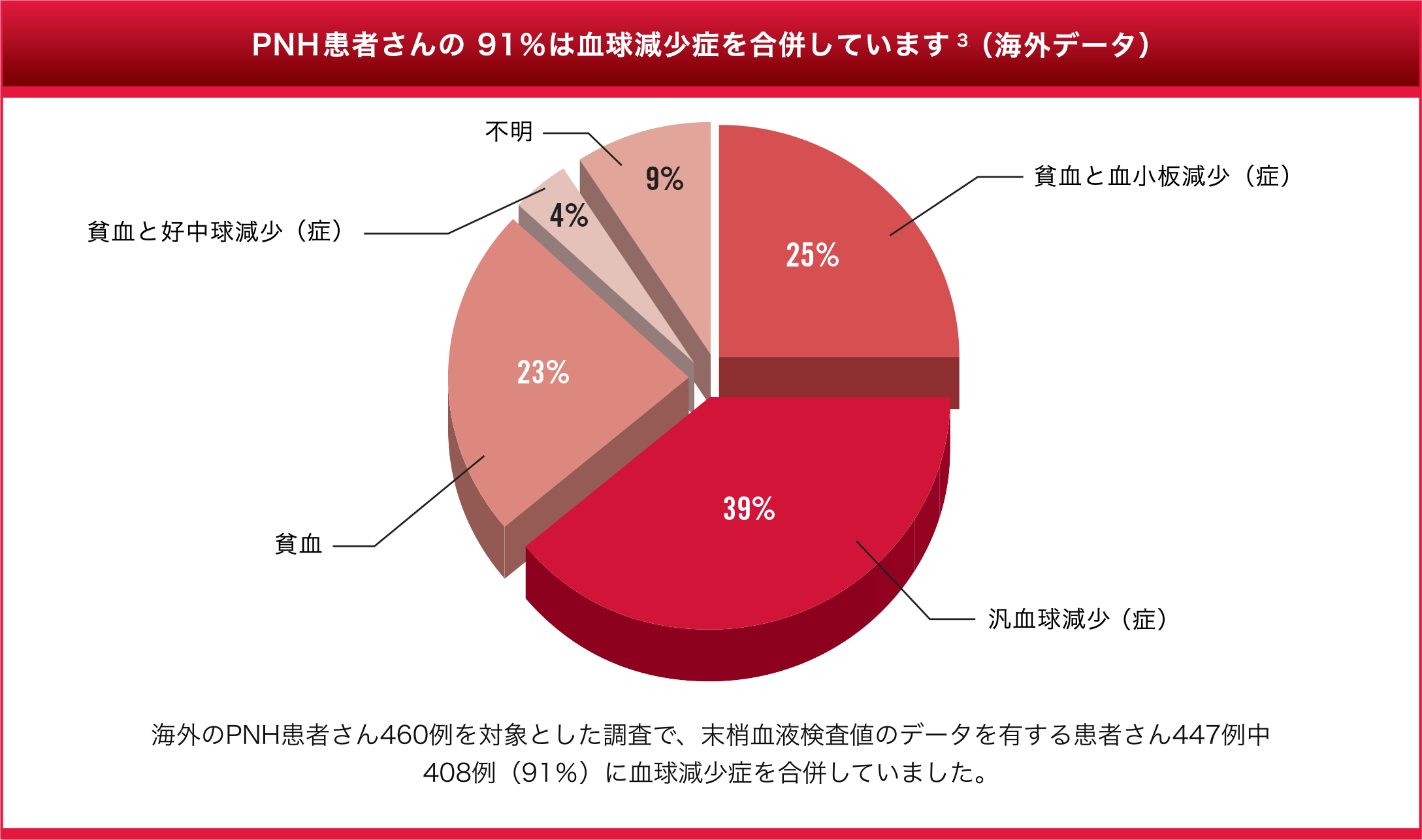
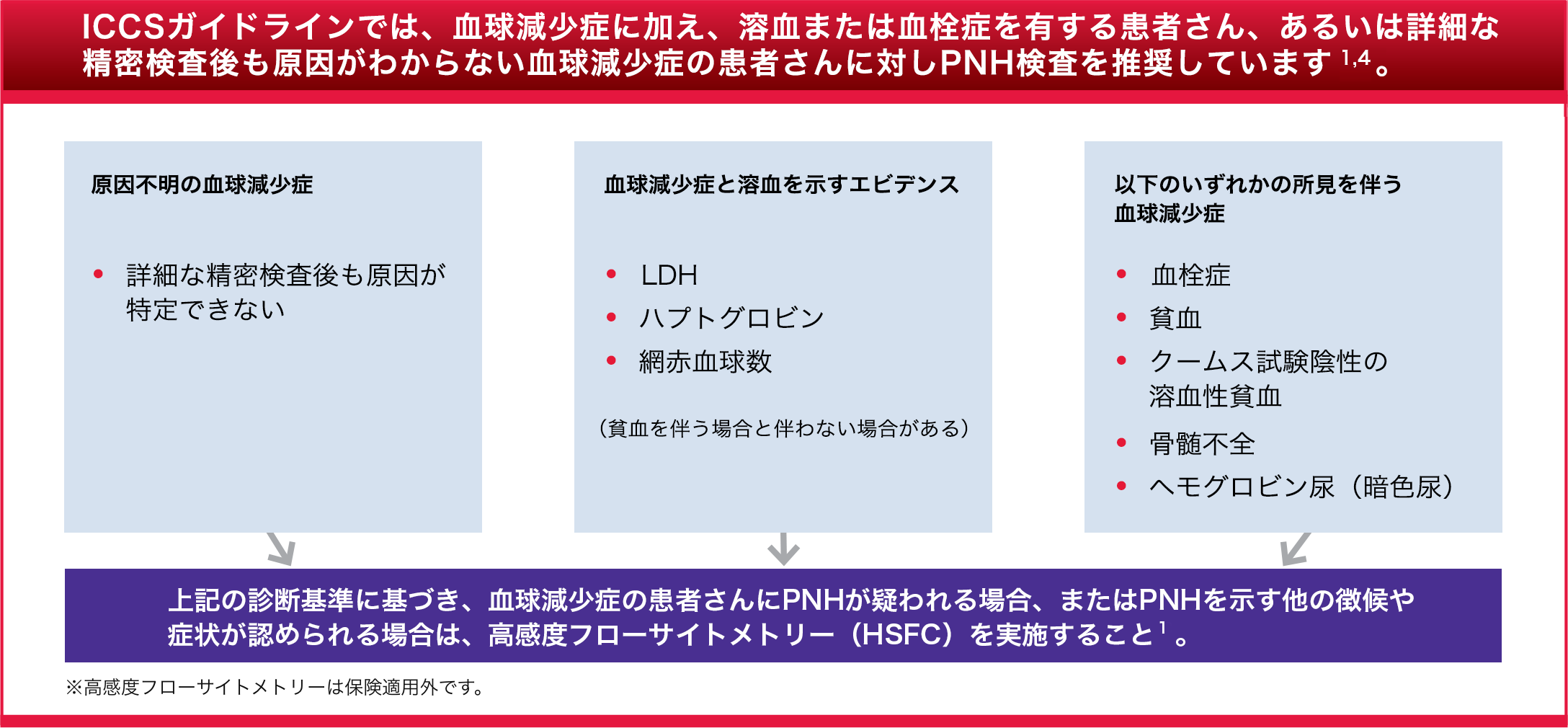
1. Borowitz MJ, et al. Cytometry B Clin Cytom. 2010;78:211-230. 2. Raza A, et al. Cytometry B Clin Cytom. 2014;86:175-182. 3. de Latour RP, et al. Blood. 2008;112:3099-3106. 4. Brodsky RA. Blood. 2009;113:6522-6527.
原因不明の血栓症の患者さんは PNHのリスクが高くなります1,3,26
- 血管内溶血と血小板活性化はPNH患者さんの合併症や死亡の主な原因です5,6
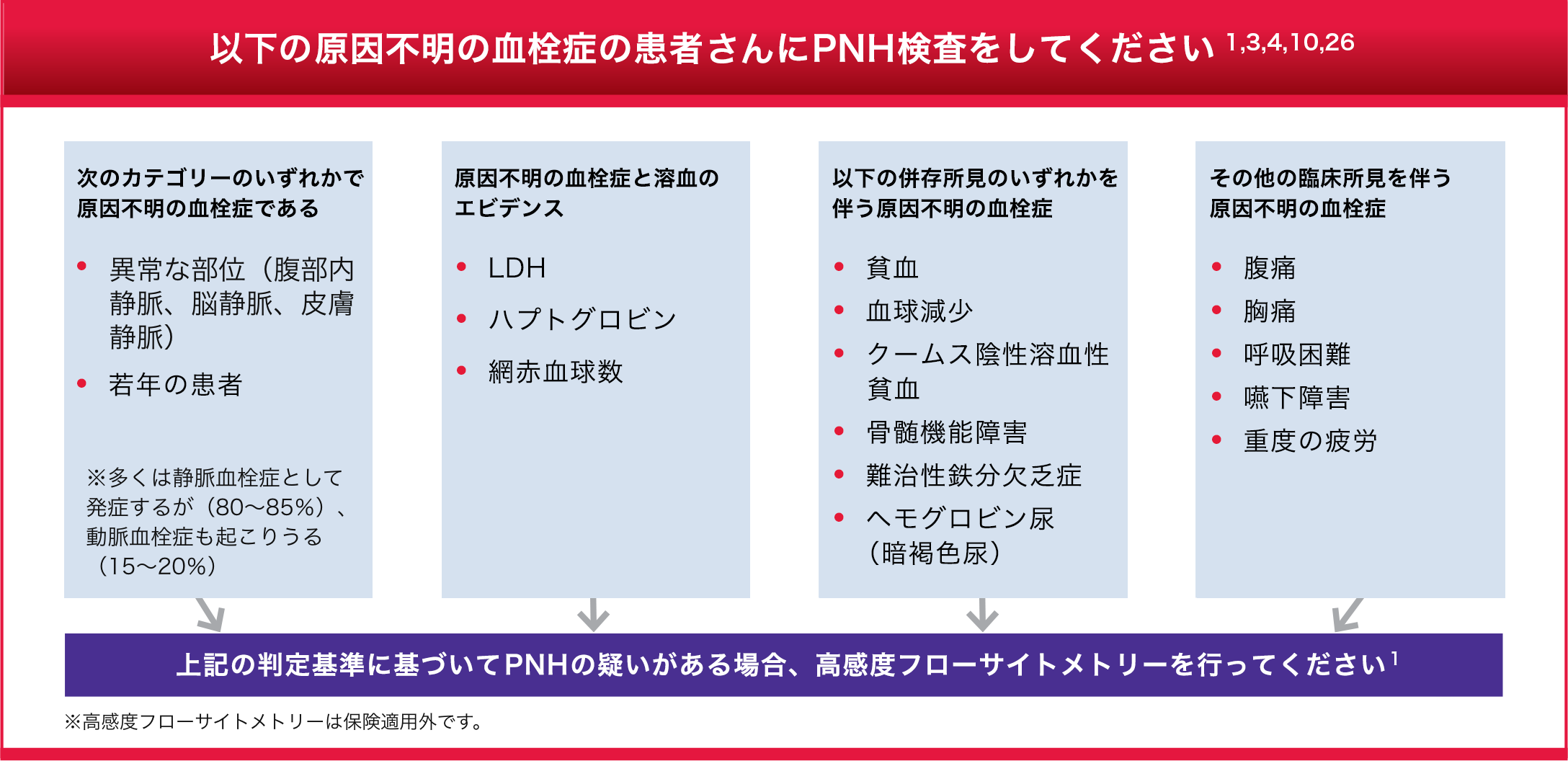
- LDH が正常値でもPNH検査を実施すべきです3
制御機能を失った補体活性化による慢性溶血によりさまざまなPNHの症状が引き起こされます11-27
- 溶血 2,7-8
- 還元型一酸化窒素(NO)
- 血小板の反応性亢進(または過剰な活性化)
- 繊維素溶解の障害
- 凝固性亢進
- 血栓形成促進性の細胞膜 3
- 還元型一酸化窒素(NO)
- CD59欠損から生じる過剰な血小板活性化 2,8
- 微小血栓形成に起因する血小板減少 9
- 組織因子による凝固は溶血とは独立している2,7
- C5a
- 炎症/凝固マーカー(D-ダイマーを含む)値の上昇
1. Borowitz MJ, et al. Cytometry B Clin Cytom. 2010;78:211-230. 2. Hill A, et al. Br J Haematol. 2007;137:181-192. 3. Hill A, et al. Blood. 2013;121:4985-4996. 4. Lee JW, et al. Int J Hematol. 2013;97:749-757. 5. Rachidi S, et al. Eur J Intern Med. 2010;21:260-267. 6. Hill A, et al. Br J Haematol. 2012;158:409-414. 7. 発作性夜間ヘモグロビン尿症診療の参照ガイド 令和4年度改訂版. 8. Helley D, et al. Haematologica. 2010;95:574-581. 9. Raza A, et al. Cytometry B Clin Cytom. 2014;86:175-182. 10. Mohanty BD, et al. Am J Med. 2012;125:243-245. 11. Parker C, et al. Blood. 2005;106:3699-3709. 12. Zipfel PF, et al. Vaccine. 2008;26(suppl 8):I67-I74. 13. Figueroa JE, Densen P. Clin Microbiol Rev. 1991;4:359-395. 14. Walport MJ. N Engl J Med. 2001;344:1058-1066. 15. Rother RP, et al. Nat Biotechnol. 2007;25:1256-1264. 16. Weitz I, et al. Intern Med J. 2013;43:298-307. 17, Hill A, et al. Br J Haematol. 2010;149:414-425. 18. Hillmen P, et al. Am J Hematol. 2010;85:553-559. 19. Hillmen P, et al. N Engl J Med. 1995;333:1253-1258. 20. Nishimura J-I, et al. Medicine (Baltimore). 2004;83:193-207. 21. Caprioli J, et al. Blood. 2006;108:1267-1279. 22. Noris M, et al. Clin J Am Soc Nephrol. 2010;5:1844-1859. 23. George JN. Blood. 2010;116:4060-4069. 24. Loirat C, et al. Pediatr Nephrol. 2008;23:1957-1972. 25. Ståhl AL, et al. Blood. 2008;111:5307-5315. 26. Hosler GA, et al. Arch Pathol Lab Med. 2003;127;834-839. 27. Ariceta G, et al. Pediatr Nephrol. 2009;24:687-696.

.png)